| 제목 | 답변완료 루이스 전자점식 | ||
|---|---|---|---|
| 질문유형 | 강좌내용 | 교수님 | 고영권 |
| 과목 | 강좌명 | ||
| 작성자 | 김*연 (d********r) | 등록일 | 2020-02-17 16:14 |
|
8강 화학 결합에서 루이스 전자점식 수강중 궁금한 점이 생겨서요. 중심 원자 기준이 크기가 크거나 결합 선이 많은 거라고 하셨는데. 결합선이 많은것은 원자번호랑 연관이 없는 부분인가요? 예제 8-1 (1)중심원자가 왜 Cl이 아니라 C인건지 ㅜ (4) 왜 N이 아닌 c가 중심원자인지 궁금합니다. 답변 완료된 질문과 답변은 수정 및 삭제가 불가합니다. |
|||
- 댓글
- 0
안녕하세요?
이해하기 쉬우라고 그렇게 설명했는데
오히려 혼동을 드린 것 같습니다.
지금 수준에서는 그냥 외우는 것이 더 쉽습니다.
사실 전기음성도도 따져야 하거든요.
이렇게 설명 드리겠습니다.
(1)번 예제 :
- Cl은 전자를 받고 싶어하고
- C는 전자를 주는 것을 더 좋아합니다.
- 그래서 C가 중심원자 입니다.
(4)번 예제 :
- 여기서도 C는 주고 싶어하고, N은 받고 싶어합니다.
- 그래서 C가 중심원자 입니다.
이해하시기 어려우시죠?
처음에는 그냥 퍼즐이라고 생각하시면 편합니다.
(1)번 예제 :
- H는 결합선이 1개인데 원자가 2개 있고
- C는 결합선이 4개인데 원자가 1개 있고
- Cl은 결합선이 1개인데 원자가 2개 있고
- 아!!! C가 가운데서 다른 원소를 잡아주면 되겠구나~
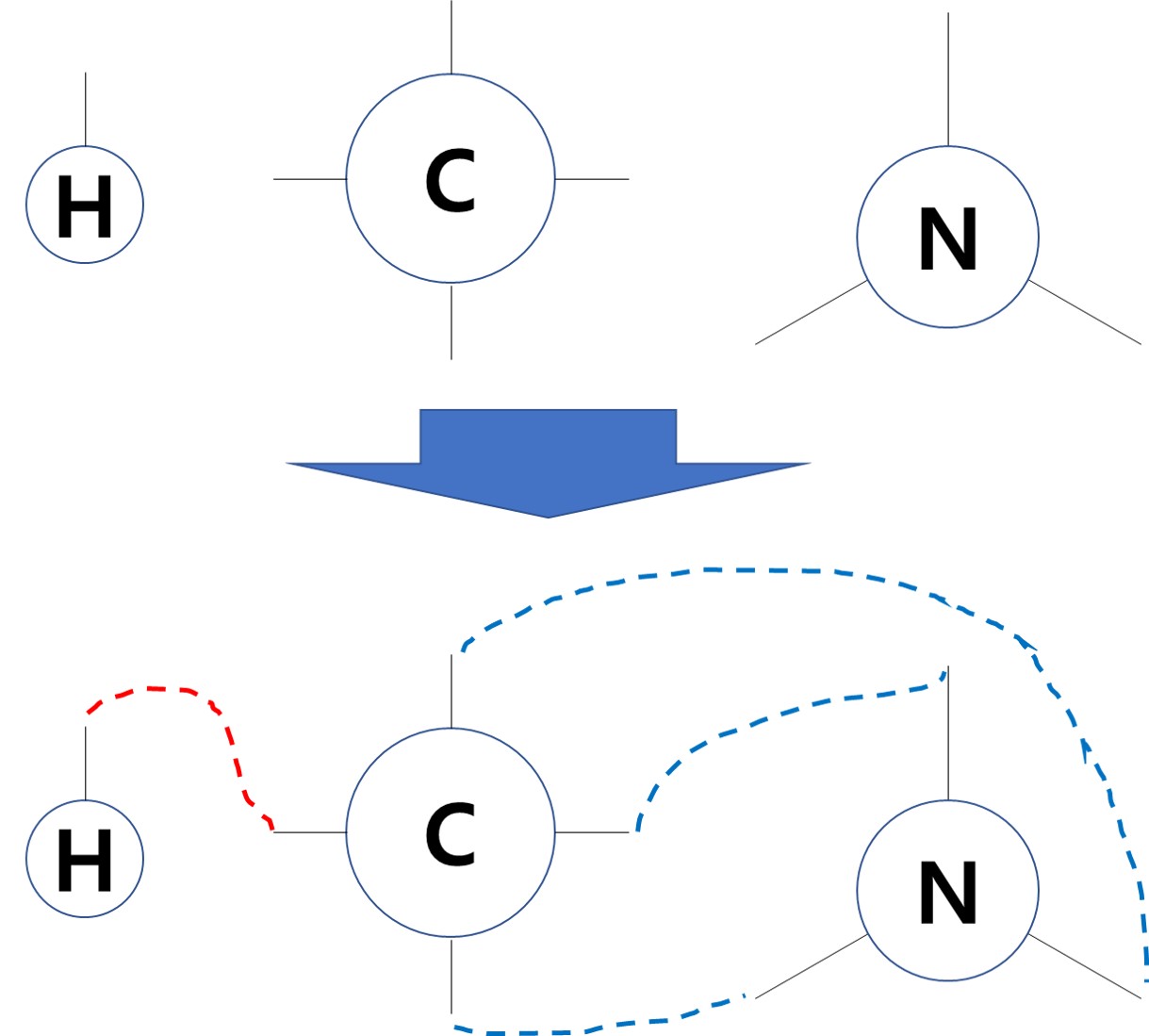
(4)번 예제 :
- H는 결합선이 1개인데 원자가 1개 있고
- C는 결합선이 4개인데 원자가 1개 있고
- N은 결합선이 3개인데 원자가 1개 있고
- 아!! C가 가운데서 다른 원소를 잡아주면 되겠구나~
아주 자세한 이론적인 내용은 인터넷에 좋은 것이 많으니, 참조 부탁 드립니다.
- 예시 : https://ywpop.tistory.com/6302
- 2020-02-17
- 2024-12-12 수정




























